| (�Q�j�^�������A�a��}�����镪�q�@���̉�
�@
������������z�������́A�킽���B�̐��̓��ɗB��C���X��������������Ă��Ȃ��i�\1�j�B���̂��߁A�C���X�����̕���@�\���j�Q���ꂽ��A�����g�D�̃C���X���������ቺ�����肷��ƁA���A�a�ɂȂ��Ă��܂��B

�@
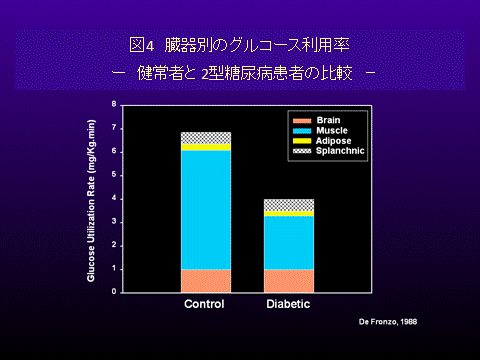
�}4�́A�C���X������p�̑傫����ʂɒ��ׂ��������ʂł���(6)�B����ҁiControl�j�ł́A����7���ȏオ���i�ŗ��p����Ă���B����A���A�a���ҁiDiabetic�j�ł́A�S�g�̑����p�ʂ�����҂̖��ɂȂ��Ă���A���̌����͍��i�i�̕����j�ł̗��p�����ቺ�������߂ł���ƕ�����B�܂�A���i�̓C���X�����̎�v�ȕW�I�ł���A�����𗘗p���Ă����ő�̑���Ƃ�����B���i���C���X������R���������i�܂�C���X���������ቺ����Ɓj�A�זE���ɓ�����肭��荞�ނ��Ƃ��ł��Ȃ��Ȃ�ƁA�s��������������������ɉߏ�ƂȂ��ē��A�a�̏Ǐ��悷��悤�ɂȂ�B
2�D�C���X�����̍זE�����`�B�@�\
�זE�́A�זE���ɂ���āA�������ƊO���������R�Ƌ�ʂ���Ă���B���̂��߁A���t���̃O���R�[�X�����i�̍זE���Ɏ�荞�ނɂ́A�זE����ʉ߂������i���K�v�ƂȂ�B������s���̂��O���R�[�X�g�����X�|�[�^�[4�iGLUT4�j�ł���i�}5�j�BGLUT4�́A�ʏ�͍זE���ɍT���Ă��邪�A����荞�݂𑣐i�����鉽�炩�̎h���������ƍזE���Ɉړ����đg�ݍ��܂�A�זE���ւ̓��̎�荞�ݒʘH�Ƃ��ē����B�h�������܂�ƁAGLUT4�͍ĂэזE���ɖ߂�A���̓����̋@���҂B
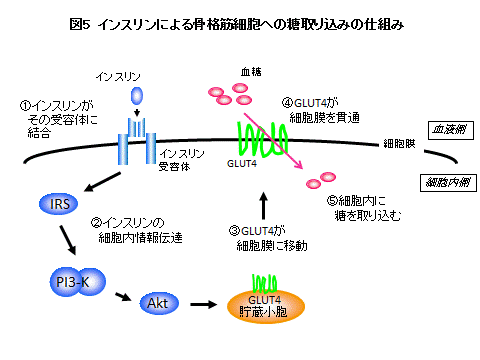
�C���X�����́A�����l�̏㏸�����m�����X�����番�傳���ƌ����ɏ���č��i�ɉ^���B���i�̍זE���\�ʂɂ���C���X������e�̂Ɍ�������ƁA���ꂪ���������ƂȂ��āA�זE���ł�IRS�API3�L�i�[�[�AAkt�Ȃǂ̏��`�B���q�����X�Ɋ����������B���̏�ŏI�I�ɍזE����GLUT4�����ɂɓ`�B����A����荞�݂��������i�}5�j�B���ꂪ�C���X�����̍זE�����`�B�ɂ�铜��荞�ݑ��i�̎d�g�݂ł���B���A�a���҂��C���X������R�������̂́A���̏��`�B�o�H�̂ǂ����i�����炭�������j���ُ���N�������߂ƍl�����Ă���B
3�D�؎��k������荞�݂����͂ɑ��i����
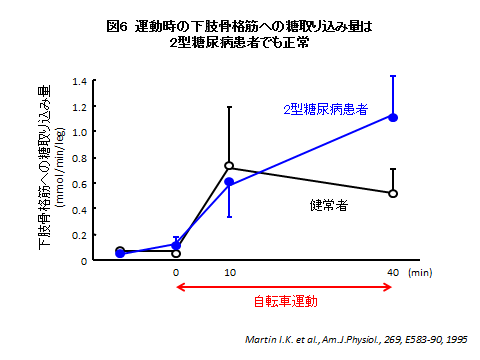
���́A���i�����k�����邱�Ƃł��A����荞�݂��N����B���̌��ʂ̓C���X�����ɕC�G���鋭�͂Ȃ��̂ł��邪�A�������Ƃɂ��̒��߂́A�C���X�����̍זE�����`�B����Ȃ��Ǝ��̌o�H�ōs����(7)�B�܂�؎��k�́A���̓��B��̌����~���z�������i�C���X�����j�Ƃ͈قȂ�����ŁA�����l��������̂ɍv������B���̂��Ƃ͔��ɏd�v�ȈӖ������B�}6�́A���]�ԉ^�����ɉ����̍��i�Ɏ�荞�܂�铜�̗ʂ��A����҂Ɠ��A�a���҂Ŕ�r�������̂ł���(8)�B���A�a���҂ł����Ă��A�^�����i�؎��k���j�ɂ͌���҂Ɠ����̓���荞�݂�������B�}4�����5�ŐG�ꂽ�悤�ɁA���A�a�́A���i�̃C���X�������`�B�o�H���s�S�ƂȂ��ē���荞�݂��j�Q���ꂽ���ʐ�����B�������A����ɓ����ʂ̌o�H�i�܂�؎��k�E�^���̌o�H�j������Ȃ��������g�p���������A�s�S�ƂȂ����o�H�����g��������L���ɓ����͂��ł���B���A�a�ɉ^�����L���ȗ��R�̈�������ɂ���B
4�D�؎��k���̓��A���߂���זE�����`�B�@�\
�ł́A�ǂ̂悤�Ȍo�H���؎��k���ɂ͓����Ă���̂��낤���B�}7�́A�����_�̍ŐV�̌������ʂ̊T���ł���B�؎��k�̏ꍇ���A�ŏI�I��GLUT4���זE���ɑg�ݍ��܂�ē��̎�荞�ݒʘH�����B�������A�����Ɏ���܂ł̏��`�B�o�H�͈قȂ�B���̎���ƂȂ���`�B���q�́AAMP�L�i�[�[��SNARK�A�����Ă����̏㗬�Ɉʒu����LKB1�����CaMKK�ł���BAMP�L�i�[�[�͍זE���G�l���M�[�Z���T�[�Ƃ��Ă�A�זE���̃G�l���M�[��Ԃ��ǍD�ȁiATP�������j�ꍇ�͕s�����^�����AATP���g�p����AMP����������Ɗ����^�ɂȂ�(7)�B�^�������i��AMP�L�i�[�[��������������(9, 10)�BLKB1��CaMKK�́AAMP�L�i�[�[�������_�����Ċ����������镪�q�ł���B
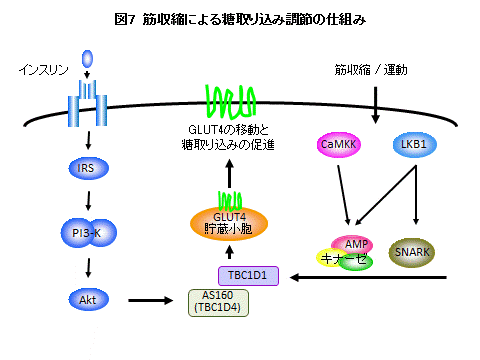
�{�������́A�@ AMP�L�i�[�[�͍זE���G�l���M�[�����������ꍇ�̗B��̓���荞�ݒ��ߕ��q�ł��邪(11)�A�A �؎��k�̏ꍇ�̓G�l���M�[����������ɂ�������炸AMP�L�i�[�[�̑j�Q�����ł͓���荞�݂�}�����邱�Ƃ͂ł��Ȃ�(11)�B�B LKB1(12)��CaMKK(13)�̓�����j�Q����Ƌ؎��k�ɂ�铜��荞�݂͗}������邱�Ƃ���A�C LKB1��CaMKK�̉����Ɉʒu����G�l���M�[�ȊO�̗v�f�Ŋ���������镪�qSNARK��AMP�L�i�[�[�ƂƂ��ɒ��߂Ɋւ���Ă���(14)�A�ƍl���Ă���B����ɂ��̉����ł́ATBC1D1(15)��AS160�iTBC1D4�j(16)���A�C���X�����Ƌ؎��k�̍זE�����������ڂ��ʂ����AGLUT4�̒������E���זE���ւƈړ�������}��q�Ƃ��ē������Ƃ���������Ă���B
5�D�؎��k�i�^���j����߂�\��
1990
�N��㔼�ɕč��ŁA���A�a�\�h�Ɋւ����K�͂ȉu�w����������s��ꂽ(17)�B�߂����A�a�ǂ���\���������Ɛf�f���ꂽ����l�̑Ώێ҂ɂ��āA���ۂ̔��Ǘ����3�N�Ԃɂ킽��ǐՒ��������̂ł���B���g�t�H���~���Ƃ������A�a���Ö�ǑO���畞�p���Ă���ƁA���Ǘ����ቺ���邱�Ƃ����������B����́A���A�a���Öu�\�h��v�Ƃ��Ă��������Ƃ������ꂽ���߂Ă̕ł������B���g�t�H���~���͉��B�ł��̌����~����p���F�߂��Ĉȗ��A���E���ōL���g�p����Ă������A�a���Ö�ł���B���������̍�p�@���͒����s���ŁA�u�Ȃ��������v�̂Ŏg�p����Ă����o�܂�����B���̌�A21���I�ɓ����Ă܂��Ȃ��A���g�t�H���~���͍��i��AMP�L�i�[�[�����������������~����p�����Ă��邱�Ƃ����炩�ɂȂ���(18)�B�܂�A���g�t�H���~���͉^���Ɠ������J�j�Y���œ��A�a�̗\�h���ʂ����Ă����̂ł���B�u�^���v�Ɓu����v�̈Ӗ����A���A�a�\�h�Ƃ��������ɂ����Ĉ�_�Ɏ��������u�Ԃł������B�����̎����́A�؎��k�i�^���j�͌����l��������z�������̂悤�ɓ������A���A�a��\�h�E���P�������̂悤�ɂ��������Ƃ������Ă���B�킽���B�͂��˂Ă���A�p���I�ɉ^������ƌ��N�ł����A�a��Ȑ������牓�������Ă�����̂ł͂Ȃ����Ɗ��Â��Ă͂����B���̔閧�̊j�S�́A�؎��k���̂��̂ɂ���̂�������Ȃ��B
6�D�����̗ʂł͂Ȃ�������� - �A�X���[�g�E�p���h�b�N�X -
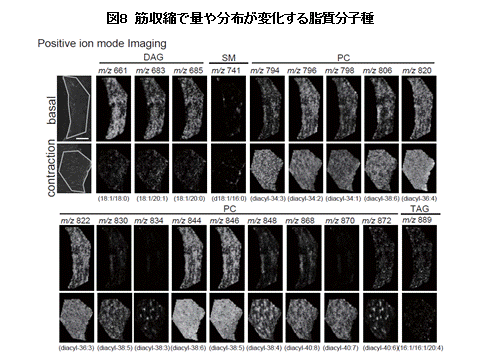
���i���C���X������R���ǂ���̂͋؍זE���ɑ�ʂ̎������~�ς��ꎖ�������A�Ƃ����̂�����Ƃ���Ă���(19)�B�������������錻�ۂ��m���Ă���B���v�n���Z�̃A�X���[�g�̓C���X�������������i�܂�C���X������R�����Ȃ��j�ɂ�������炸�A�؍זE���̎����ʂ������B������A�X���[�g�E�p���h�b�N�X�ł���(20)�B�{�������ł͏]���̎��ʕ��͖@�ɉ����A���ʕ��͂�����ɐi�����������ʌ������Ƃ�������I�Ȏ�@��p����(20)�A���̃p���h�b�N�X�̓�ɔ����Ă���(21)�B���ʌ������ŋؓ��ɂ��鎉�����q��̕��z���摜�����A����E��ʂ��邱�Ƃ��ł���B����������̎������q����@�ɓ����ɉ�͂��邱�Ƃ��\�ł���B���̃A�v���[�`��p���邱�ƂŁA�ؓ��̎����͋؎��k�ɂ���Č������邾���łȂ��A�������镨���������邱�Ƃ����������B����Ɏ����̕��z�͎�ނɂ���ē����I�ő��l�ł��邱�Ƃ����炩�ɂȂ����B���Ȃ킿�A�C���X������R���͒P�Ɏ����̗ʂŌ��܂�̂ł͂Ȃ��A�זE���ɒ~�ς��鎉���̎�ނ₻�̕��z���d�v�ł��邱�Ƃ����������B
����
6. DeFronzo
R.A., The triumvirate: b-cell, muscle, liver. A collusion responsible for NIDDM., Diabetes
, 37, 667-87, 1988
7. Fujii
N, Jessen N, Goodyear LJ. AMP-activated
protein kinase and the regulation of glucose transport. Am J Physiol Endocrinol Metab.
291(5):E867-77. 2006
8. Martin
IK., Katz A, Wahren J., Splanchnic and muscle metabolism during exercise in
NIDDM patients., Am.J.Physiol., 269, E583-90, 1995
9. Fujii
N, Hayashi T, Hirshman MF, Smith JT, Habinowski SA, Kaijser L, Mu J, Ljungqvist
O, Birnbaum MJ, Witters LA, Thorell A, Goodyear LJ. Exercise induces isoform-specific increase in
5'AMP-activated protein kinase activity in human skeletal muscle. Biochem
Biophys.Res.Commun. 273(3):1150-5. 2000
10. Musi
N, Fujii N, Hirshman MF, Ekberg I, Froberg S, Ljungqvist O, Thorell A, Goodyear
LJ. AMP-activated protein kinase (AMPK) is activated in muscle of subjects with
type 2 diabetes during exercise.
Diabetes. 50(5):921-7. 2001
11. Fujii
N, Hirshman MF, Kane EM, Ho RC, Peter LE, Seifert MM, Goodyear LJ. AMP-activated
protein kinase a2 activity
is not essential for contraction-and hyperosmolarity-induced glucose transport
in skeletal muscle. J.Biol.Chem., 280, 29033-41, 2005
12. Koh H.
et al., Skeletal muscle-selective knockout of LKB1 increases insulin
sensitivity, improves glucose homeostasis, and decreases TRB3. Mol.Cell Biol., 26,
8217-27, 2006
13. Witczak CA, Fujii N, Hirshman MF,
Goodyear LJ., Ca2+/calmodulin-dependent
protein kinase kinase-a regulates skeletal muscle glucose
uptake independent of AMP-activated protein kinase and Akt activation. Diabetes, 56, 1403-9, 2007
14. Koh
HJ, Toyoda T, Fujii N, Jung MM, Rathod A, Middelbeek RJ, Lessard SJ, Treebak
JT, Tsuchihara K, Esumi H, Richter EA, Wojtaszewski JF, Hirshman MF, Goodyear
LJ. Sucrose nonfermenting AMPK-related kinase (SNARK) mediates
contraction-stimulated glucose transport in mouse skeletal muscle. Proc Natl
Acad Sci U S A. 107(35):15541-6, 2010
15. An D,
Toyoda T, Taylor EB, Yu H, Fujii N, Hirshman MF, Goodyear LJ. TBC1D1 regulates insulin- and
contraction-induced glucose transport in mouse skeletal muscle. Diabetes. 59(6):1358-65, 2010
16. Taylor
EB, An D, Kramer HF, Yu H, Fujii NL, Roeckl KS, Bowles N, Hirshman MF, Xie J,
Feener EP, Goodyear LJ. Discovery of
TBC1D1 as an insulin-, AICAR-, and contraction-stimulated signaling nexus in
mouse skeletal muscle. J Biol Chem. 283(15):9787-96. 2008
17. Diabetes
Prevention Program Research Group: Reduction in the incidence of type 2 diabetes with lifestyle
intervention or metformin. N.Engl.J.Med., 346, 393-403,
2002
18. Zhou
G. et al., Role of AMP-activated protein kinase in mechanism of metformin
action. J.Clin.Invest. 108, 1167-74,
2001
19. Fujii
N, Ho RC, Manabe Y, Jessen N, Toyoda T, Holland WL, Summers SA, Hirshman MF,
Goodyear LJ. Ablation of AMP-activated
protein kinase alpha2 activity exacerbates insulin resistance induced by
high-fat feeding of mice. Diabetes.
57(11):2958-66. 2008
20. Goto-Inoue
N, Setou M, Fujii NL. Visualization of
metabolite change in skeletal muscle by contraction using imaging mass
spectrometry. J.Phys.Fit.Sport.Med., 1(2): 347-50. 2012
21. Goto-Inoue N, Manabe Y, Miyatake S, Ogino S, Morishita A, Hayasaka T, Masaki
N, Setou M, Fujii NL. Visualization of dynamic change in contraction-induced
lipid composition in mouse skeletal muscle by matrix-assisted laser desorption/ionization
imaging mass spectrometry. Anal Bioanal Chem. 403(7):1863-71. 2012
�ŋ߂̔��\�_��
�@�@�@�P�DInada A�CFujii NL�CNabeshima YI�Cet al�D Adjusting the 17��-Estradiol-to-Androgen Ratio Ameliorates Diabetic Nephropathy�D J ournal of American Society of Nephrology�C 28(2):716�C 2017�N�D
�Q�DYu H�CFujii NL�CToyoda T�CHirshman MF�CGoodyear LJ�C et al
Contraction stimulates muscle glucose uptake independent of atypical PKC�D Physiological Reports�C 3(11)�C e12565�C 2016�N�D
|